去年年底,中國(guó)科學(xué)院生物化學(xué)與細(xì)胞生物學(xué)研究所的周斌團(tuán)隊(duì)與交通大學(xué)國(guó)際婦幼保健院的黃荷鳳團(tuán)隊(duì)在Circulation期刊上發(fā)表了題為“In Vivo AAV-CRISPR/Cas9-mediated Gene Editing Ameliorates Atherosclerosis in Familial Hypercholesterolemia”的文章,發(fā)現(xiàn)利用AAV-CRISPR/Cas9系統(tǒng)對(duì)攜帶可導(dǎo)致家族性高膽固醇血癥(FH)的致病Ldlr突變小鼠進(jìn)行LDLR基因校正,能夠部分地修復(fù)低密度脂蛋白受體(LDLR)表達(dá)并有效改善LDLR突變體中的動(dòng)脈粥樣硬化,為FH患者的治療提供潛在的治療方法。
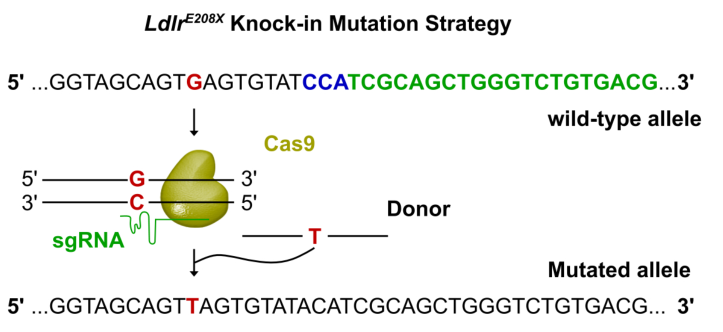
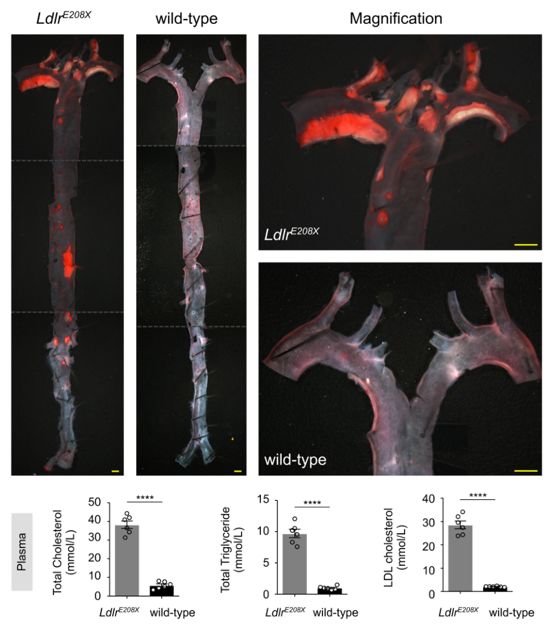
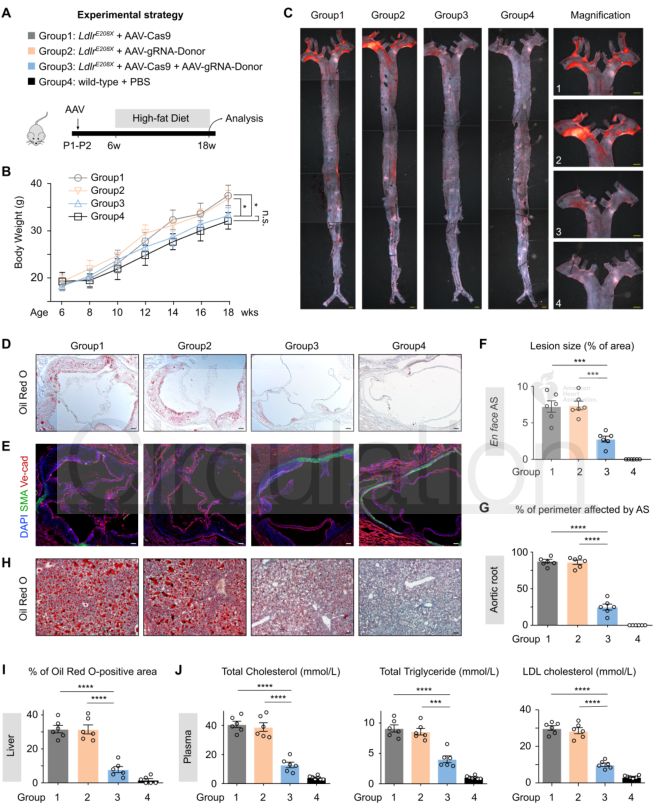
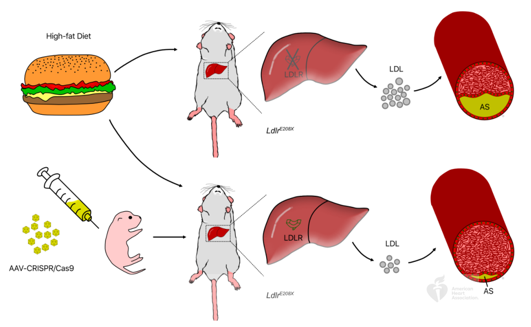
Innovation 創(chuàng)新點(diǎn) 1. 為人類家族性高膽固醇血癥發(fā)病機(jī)制的研究建立了一種新的模型:含E208X無義點(diǎn)突變的LdlrE208X小鼠。 2. 通過單次注射AAV-CRISPR/Cas9對(duì)LdlrE208X小鼠進(jìn)行體內(nèi)基因編輯,可以減少脂質(zhì)積累并改善動(dòng)脈粥樣硬化。 背景介紹 家族性高膽固醇血癥(FH)的特點(diǎn)是低密度脂蛋白膽固醇(LDL-C)水平顯著升高和過早發(fā)生心血管疾病。FH是一種常染色體顯性遺傳病,具有基因劑量效應(yīng),由編碼低密度脂蛋白受體(LDLR)、載脂蛋白B(APOB)或枯草溶菌素轉(zhuǎn)化酶9(PCSK9)的基因突變引起的。其中,90%的FH是由LDLR突變導(dǎo)致的。LDLR突變可導(dǎo)致功能性LDLR的表達(dá)水平降低,肝臟對(duì)血液循環(huán)中LDL-C的清除能力下降,進(jìn)而使血液循環(huán)中的LDL-C過量,從而導(dǎo)致動(dòng)脈粥樣硬化斑塊的發(fā)生和發(fā)展。動(dòng)脈粥樣硬化的嚴(yán)重程度與肝組織中LDLR的表達(dá)水平和活性密切相關(guān)。 純合子FH(HoFH)的發(fā)病率約為百萬分之一,可在嬰幼兒時(shí)期就迅速發(fā)展為嚴(yán)重的動(dòng)脈粥樣硬化和心血管疾病,并導(dǎo)致死亡。雜合子FH患者(HeFH)具有功能性LDLR蛋白,因此目前的FH藥物治療(例如MG-CoA還原酶抑制劑(他汀類))通常只對(duì)HeFH有效,而高強(qiáng)度他汀類藥物和PCSK9抑制劑對(duì)HoFH的治療效果非常有限。這些差異表明即使低水平的LDLR表達(dá)和活性也可以顯著影響FH的嚴(yán)重程度和發(fā)展速度。針對(duì)HoFH,現(xiàn)有的治療手段包括LDL血漿置換及肝移植等,費(fèi)用昂貴且存在一定風(fēng)險(xiǎn),因此繼續(xù)尋找和探索新的治療方法具有重要意義。 關(guān)于家族性高膽固醇血癥臨床特征及相關(guān)基因檢測(cè)的更多介紹,詳見(點(diǎn)擊查看原文): 《Nature review的最新綜述:設(shè)計(jì)家族性高膽固醇血癥的適應(yīng)性護(hù)理模式所需的相關(guān)知識(shí)更新》 成簇規(guī)律間隔的短回文重復(fù)序列(CRISPR)和其相關(guān)核酸內(nèi)切酶(Cas)是近些年來發(fā)現(xiàn)和興起的一種基因編輯技術(shù),以其高效性和簡(jiǎn)便性廣泛應(yīng)用于不同物種的細(xì)胞基因編輯、動(dòng)物模型構(gòu)建和致病基因治療等方面,極大地促進(jìn)了生物學(xué)和醫(yī)學(xué)研究發(fā)展。腺相關(guān)病毒(AAV)由于其高安全性以及穩(wěn)定長(zhǎng)效表達(dá),被視為最有前景的基因治療載體。利用AAV進(jìn)行的基因治療目前已被批準(zhǔn)用于80多種疾病,并已用于臨床試驗(yàn)。利用基因治療人類遺傳疾病是近年來醫(yī)學(xué)生物領(lǐng)域的熱點(diǎn)課題。 本研究為了確定AAV介導(dǎo)的CRISPR/Cas9系統(tǒng)對(duì)體內(nèi)體細(xì)胞進(jìn)行基因編輯是否可治療由Ldlr突變引起的FH。 研究方法及結(jié)果 研究人員根據(jù)已在FH患者中發(fā)現(xiàn)的LDLR基因E207X無義突變(提前產(chǎn)生終止密碼子,導(dǎo)致LDLR蛋白無法正常表達(dá)),利用CRISPR/Cas9系統(tǒng)將其導(dǎo)入小鼠受精卵進(jìn)行打靶(圖1),通過后續(xù)傳代交配,成功構(gòu)建LdlrE208X小鼠(純合子),并通過基因測(cè)序、反轉(zhuǎn)錄PCR、Western blot和免疫熒光染色等方法進(jìn)行了驗(yàn)證。結(jié)果發(fā)現(xiàn)攜帶純合突變的LdlrE208X小鼠(n=6)經(jīng)高脂膳食喂養(yǎng)后,肝臟中無LDLR蛋白表達(dá),表現(xiàn)為嚴(yán)重的動(dòng)脈粥樣硬化表型(圖2),與人類的HoFH患者表現(xiàn)類似。 圖1. LdlrE208X敲入小鼠的突變策略。 圖2. 高脂膳食喂養(yǎng)后LdlrE208X小鼠主動(dòng)脈動(dòng)脈粥樣硬化病變的油紅O染色圖像及血漿總膽固醇、總甘油三酯、低密度脂蛋白(LDL)膽固醇水平對(duì)比。 隨后利用AAV將CRISPR/Cas9系統(tǒng)(AAV-CRISPR/Cas9)送入LdlrE208X小鼠(n=6)體內(nèi),通過小向?qū)NA(sgRNA)引導(dǎo)Cas9蛋白至特定DNA位點(diǎn)后,利用同源重組修復(fù)(HDR)來矯正部分肝細(xì)胞的Ldlr突變,并部分恢復(fù)其LDLR蛋白的表達(dá)(n=6)。與對(duì)照組(n=6)相比,sgRNA的AAV-CRISPR/Cas9組(每組6只)的血清總膽固醇、總甘油三酯和LDL-C均顯著降低,且主動(dòng)脈粥樣硬化斑塊更小,巨噬細(xì)胞浸潤(rùn)程度更低,LdlrE208X小鼠肝臟脂肪蓄積得到有效降低(圖3和圖4)。同時(shí)CRISPR/Cas9系統(tǒng)的脫靶效應(yīng)和一些免疫指標(biāo)均顯示,成體小鼠體內(nèi)并未發(fā)現(xiàn)明顯的脫靶及免疫排斥反應(yīng),支持了此次基因編輯治療的有效性和安全性。 圖3. AAV-CRISPR/Cas9治療后LdlrE208X小鼠中LDLR表達(dá)的部分恢復(fù)和動(dòng)脈粥樣硬化的改善。 A. 腺相關(guān)病毒(AAV)注射、高脂飲食喂養(yǎng)及分析的實(shí)驗(yàn)策略。B. 各組不同時(shí)期的體重。C. 主動(dòng)脈動(dòng)脈粥樣硬化病變的油紅O染色圖像。D. 小鼠主動(dòng)脈根部油紅O染色圖像。E. 主動(dòng)脈根部平滑肌肌動(dòng)蛋白(SMA)和Ve-cad的免疫染色。F. 各組動(dòng)脈粥樣硬化病變面積的量化。G. 各組動(dòng)脈粥樣硬化(AS)對(duì)主動(dòng)脈周長(zhǎng)的影響。H. 肝切片油紅O染色圖像。I. 肝切片油紅O陽性區(qū)的定量。J. 小鼠血漿總膽固醇、總甘油三酯、低密度脂蛋白膽固醇水平對(duì)比。 圖4. AAV-CRISPR/Cas9治療后LdlrE208X小鼠的部分恢復(fù)及動(dòng)脈粥樣硬化表型改善的示意圖。 以上結(jié)果表明,通過AAV-CRISPR/Cas9系統(tǒng)進(jìn)行的體內(nèi)基因編輯可能是一種有效的HoFH治療方法,同時(shí)可能有助于改善當(dāng)前降脂藥物的療效。此外也證明CRISPR/Cas9技術(shù)可作為一種應(yīng)用于人類遺傳病治療的潛在工具,但在進(jìn)入臨床實(shí)驗(yàn)前還必須進(jìn)行更多研究測(cè)試(如大型動(dòng)物試驗(yàn)等)。 結(jié)論 本研究表明在體內(nèi)用AAV-CRISPR/Cas9介導(dǎo)的Ldlr基因校正可部分恢復(fù)LDLR的表達(dá),有效改善Ldlr突變小鼠的動(dòng)脈粥樣硬化表型,為FH患者提供了一種潛在的治療方法。隨著全基因組測(cè)序成本的降低,對(duì)家庭成員和胎兒進(jìn)行篩查將變得更加普遍。因此,在疾病進(jìn)展的早期階段診斷FH,有可能實(shí)現(xiàn)通過基因校正進(jìn)行早期治療。將來,AAV-CRISPR/Cas9系統(tǒng)可能用于校正遺傳性心血管病中的一些生殖細(xì)胞基因突變,從而改善甚至修復(fù)疾病。 【參考文獻(xiàn)】 Huan Zhao, et al. In Vivo AAV-CRISPR/Cas9-Mediated Gene Editing Ameliorates Atherosclerosis in Familial Hypercholesterolemia. Circulation. 2020, 141: 67-79.