


PLD1雙等位基因功能缺失變異導(dǎo)致先天性
右側(cè)心臟瓣膜缺損和新生兒心肌病
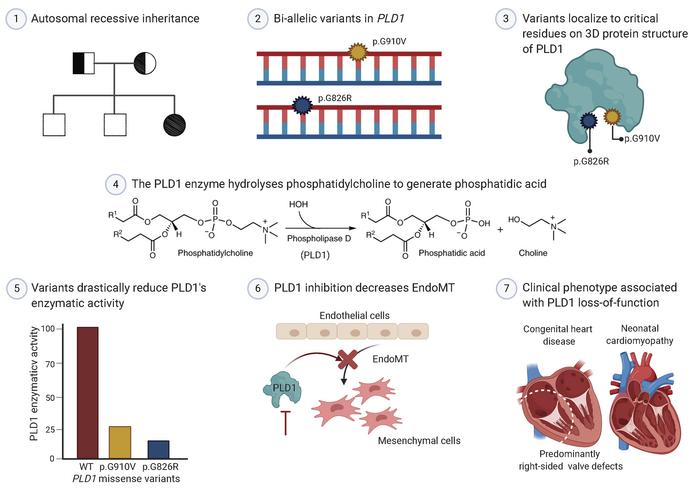
近期,Lahrouchi等對(duì)2718名先天性心臟病患者進(jìn)行全外顯子組測(cè)序(WES),并在GeneMatcher中搜索,確定了來自21個(gè)不相關(guān)家系的30名攜帶PLD1雙等位基因變異的患者(主要表現(xiàn)為先天性心臟瓣膜缺損)。并且,將常染色體隱性遺傳的PLD1基因變異與孤立性新生兒心肌病聯(lián)系起來。此外,還證實(shí)了p.I668F是德系猶太人的奠基者變異(等位基因頻率約2%),描述了PLD1相關(guān)先天性心臟缺陷的表型譜。PLD1的錯(cuò)義變異在對(duì)催化活性至關(guān)重要的蛋白區(qū)域過表達(dá)。同時(shí),PLD1抑制降低了內(nèi)皮間充質(zhì)轉(zhuǎn)化,這是瓣膜形成的關(guān)鍵早期步驟。
背景介紹
先天性心臟病是最常見的出生缺陷,占所有先天性異常的三分之一,在世界范圍內(nèi)每1000名活產(chǎn)嬰兒中有7人患有先天性心臟病。大多數(shù)缺陷包含瓣膜形成異常,右側(cè)先天性心臟病包括肺動(dòng)脈瓣和三尖瓣、右心室和右心室流出道的異常。最近,在2個(gè)小家庭中發(fā)現(xiàn)PLD1與嚴(yán)重的右側(cè)先天性心臟瓣膜缺損相關(guān)。PLD1基因編碼磷脂酶D1,該酶是一種信號(hào)轉(zhuǎn)導(dǎo)酶,可水解膜脂質(zhì)磷脂酰膽堿產(chǎn)生脂質(zhì)第二信使磷脂酸。
研究對(duì)象
研究納入了來自荷蘭國(guó)家先天性心臟缺陷登記和DNA庫(CONCOR)的75名不相關(guān)的患有嚴(yán)重右側(cè)先天性心臟瓣膜病(即三尖瓣閉鎖或狹窄、Ebstein’s異常或肺動(dòng)脈閉鎖)患者,以及來自兒童心臟基因組學(xué)聯(lián)合會(huì)(PCGC)并接受過WES檢測(cè)的2643名先天性心臟病患者(包含患者和父母雙方),共2718例。
研究方法
cDNA 分析;質(zhì)粒構(gòu)建、細(xì)胞系和轉(zhuǎn)染;體外細(xì)胞PLD活性;蛋白質(zhì)印跡分析;體外膠原蛋白凝膠實(shí)驗(yàn);PCA確定PCGC先天性心臟病病例的譜系;單倍型分析和變異年代測(cè)定等。
研究結(jié)果
·在多個(gè)家系中,PLD1變異可導(dǎo)致先天性瓣膜缺陷或新生兒心肌病
對(duì)2718名患者進(jìn)行分析,確定了來自21個(gè)不同祖先的不相關(guān)家系的30名攜帶純合或復(fù)合雜合PLD1變異的患者。這30名患者在胎兒期或新生兒期均診斷為嚴(yán)重先天性心臟病或心肌病(見圖1)。所有家系中都表現(xiàn)為常染色體隱性遺傳模式,且PLD1變異均來自未受影響的父母。其中,來自19個(gè)家系的28名患者表現(xiàn)為先天性心臟瓣膜畸形,主要影響右側(cè)心臟。值得注意的是,有2名患者表現(xiàn)為嚴(yán)重孤立性新生兒心肌病(即無結(jié)構(gòu)性先天性心臟缺陷)(見圖1A,F(xiàn)amilies T 和 U),這是該綜合征的新發(fā)現(xiàn)。對(duì)這2名患者進(jìn)行了約300個(gè)心肌病相關(guān)基因變異的篩查,結(jié)果均為陰性。總體而言,嬰兒期后存活的患者均未出現(xiàn)畸形、智力殘疾或顯著的發(fā)育遲緩,這表明在明顯的表型背景下,PLD1功能缺失主要與人類孤立性心臟病有關(guān)。
同時(shí),3個(gè)德系猶太人家系中都攜帶PLD1 p.I668F純合變異(見圖1A,F(xiàn)amilies G、 H 和 I)。通過PCA分析,證實(shí)了p.I668F是德系猶太人的奠基者變異。有趣的是,p.I668F在gnomAD德系猶太人亞群中的MAF約為2%,而在其他人群中很少見(0.004%-0.14%)。
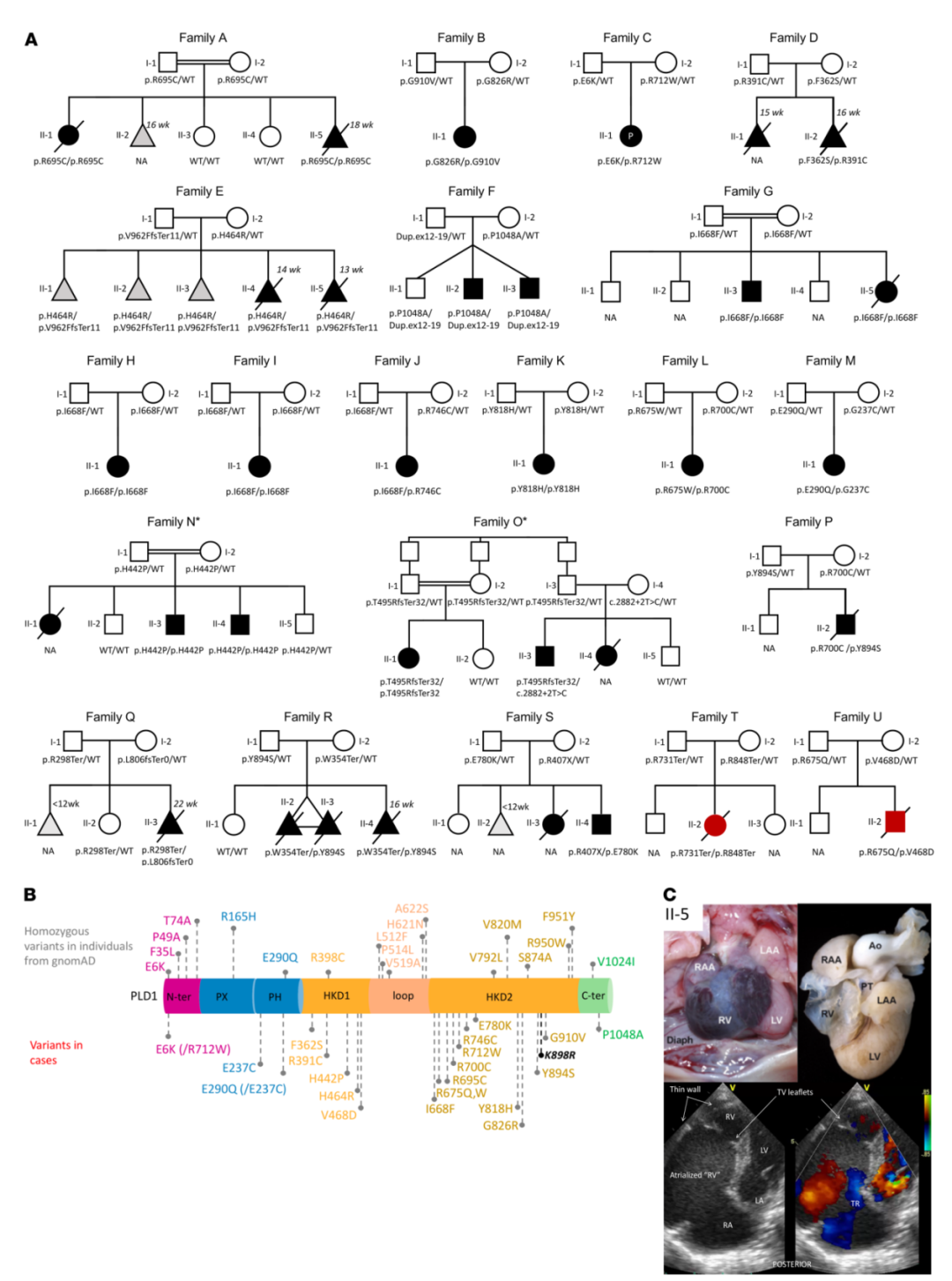
圖1. PLD1常染色體隱性變異可引起一系列
先天性心臟瓣膜病和新生兒心肌病
·PLD1的錯(cuò)義變異導(dǎo)致酶活性降低
上述21個(gè)錯(cuò)義變異主要聚集在PLD1高度保守的HxKxxxxD(HKD)域和C末端區(qū)域,這些區(qū)域?qū)γ富钚灾陵P(guān)重要(見圖1B)。酶活性試驗(yàn)顯示,在檢測(cè)的19個(gè)變異中有17個(gè)變異的PLD1酶活性明顯下降,與野生型PLD1等位基因個(gè)體相比,攜帶雙等位基因PLD1變異的個(gè)體的PLD1活性一般低于25%(見圖2)。由于完整的C末端是酶活性所必需的,因此預(yù)測(cè)所有導(dǎo)致PLD1蛋白過早終止的變異都將完全消除PLD1酶活性,例如患有孤立性心肌病的Families T中的p.R731Ter /p.R848Ter。值得注意的是,另一位孤立性心肌病(Families U)的患者攜帶復(fù)合雜合變異(p.V468D / p.R675Q),酶催化活性大大降低(與WT相比降低了2.7%)。因此,存在PLD1變異的孤立性心肌病患者的殘留PLD1酶活性與心臟結(jié)構(gòu)畸形患者相似。
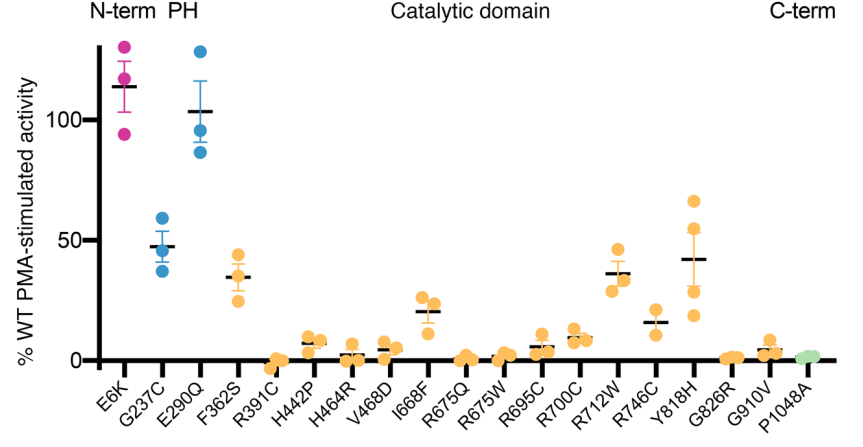
圖2. 致病性PLD1基因變異的酶活性
·在房室墊外植體中,需要PLD1來實(shí)現(xiàn)心內(nèi)膜細(xì)胞內(nèi)皮間充質(zhì)轉(zhuǎn)化
PLD1功能缺失患者的主要畸形是結(jié)構(gòu)性房室(AV)瓣膜缺損。在胚胎心臟中,覆蓋在心室前墊上的心內(nèi)膜細(xì)胞亞群經(jīng)歷了瓣膜形成的關(guān)鍵早期步驟—內(nèi)皮間充質(zhì)轉(zhuǎn)化(EndoMT)。這些間充質(zhì)細(xì)胞形成墊子,導(dǎo)致細(xì)胞外基質(zhì)的重塑,并促進(jìn)瓣膜和心臟間隔的發(fā)育。迄今為止,已經(jīng)使用體外膠原蛋白凝膠測(cè)定系統(tǒng)鑒定了許多重要的EndoMT基因,并通過該方法證實(shí)了PLD1在體外參與了內(nèi)皮間充質(zhì)轉(zhuǎn)化。異常的EndoMT至少是PLD1雙等位基因功能缺失變異心臟結(jié)構(gòu)畸形的部分原因。
結(jié)論
該研究建立了一個(gè)來自21個(gè)不相關(guān)家系的30名攜帶PLD1常染色體隱性變異的患者組成的隊(duì)列,擴(kuò)展了與PLD1相關(guān)的先天性心臟缺陷的表型譜;首次提出在沒有先天性心臟缺陷的情況下,PLD1常染色體隱性變異也可引起新生兒心肌病;同時(shí),發(fā)現(xiàn)p.I668F是德系猶太人的奠基者變異;還證實(shí)了部分PLD1的錯(cuò)義變異導(dǎo)致酶活性降低,以及PLD1參與了心內(nèi)膜細(xì)胞內(nèi)皮間充質(zhì)轉(zhuǎn)化。這些數(shù)據(jù)提供了對(duì)與PLD1遺傳缺陷相關(guān)的疾病機(jī)制和表型表達(dá)的進(jìn)一步理解。
參考文獻(xiàn):
Najim Lahrouchi, et al. Biallelic loss-of-function variants in PLD1 cause congenital right-sided cardiac valve defects and neonatal cardiomyopathy. J Clin Invest. 2021 Mar 1;131(5):e142148.
關(guān)于心肌病及相關(guān)檢測(cè)的更多介紹,詳見:
《TTN基因上的截短變異導(dǎo)致擴(kuò)張型心肌病的臨床表型和預(yù)后》
《Nature子刊最新研究——常見的遺傳變異和可改變的危險(xiǎn)因素是肥厚型心肌病易感性和表達(dá)性的基礎(chǔ)》
《CSRP3 p.(Cys150Tyr)變異與雜合個(gè)體的遲發(fā)性肥厚型心肌病相關(guān)》
《運(yùn)動(dòng)越多,肥厚型心肌病患者的死亡率越低——〈英國(guó)運(yùn)動(dòng)醫(yī)學(xué)雜志〉的最新研究》